信息来源:www.worldbrom.com | 发布时间:2025年08月06日
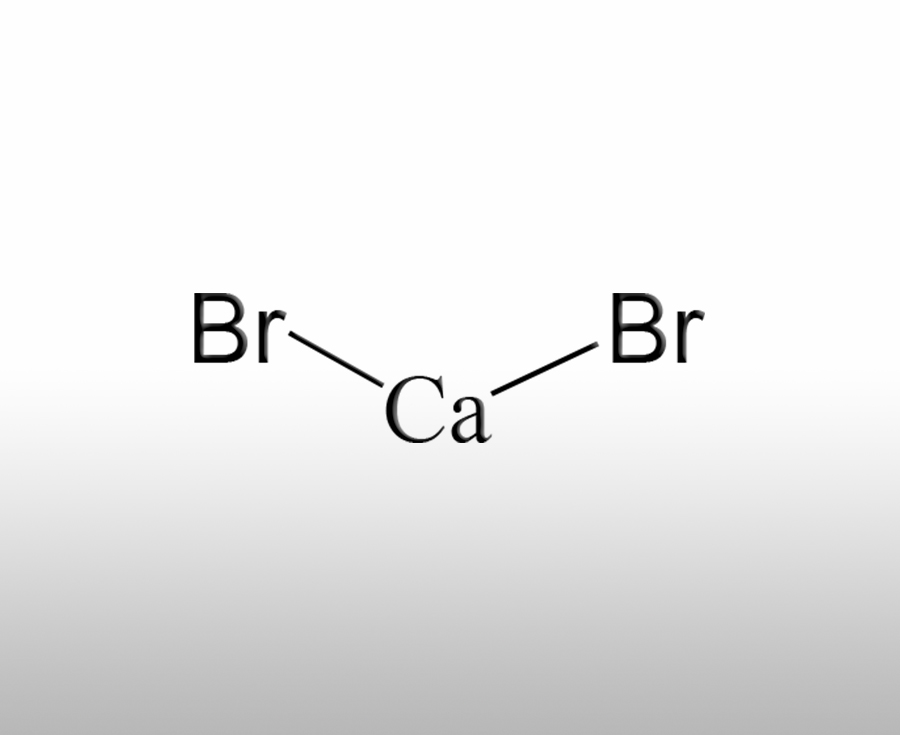
溴化钙(CaBr₂)是一种重要的无机溴化物,具有独特的化学性质和广泛的应用场景,其主要特点如下:
1. 化学性质稳定,易溶于水
溴化钙是离子型化合物,由 Ca²⁺和 Br⁻构成,常温下为白色结晶或颗粒状固体,无臭、味咸微苦。
具有极强的水溶性,且溶解度随温度升高显著增加(20℃时溶解度约 143g/100mL 水),其水溶液呈中性或弱碱性。
稳定性较好,在干燥空气中不易分解,但遇水会潮解,因此需密封保存;高温下可分解为溴化氢和氧化钙。
2. 具有镇静与神经抑制作用
溴离子(Br⁻)是中枢神经系统的抑制剂,溴化钙进入人体后可解离出 Br⁻,通过降低神经细胞的兴奋性,发挥镇静、催眠和抗惊厥作用。
医学上曾用于医治神经衰弱、癫痫、失眠等,但因副作用(如蓄积中毒、影响甲状腺功能),目前临床应用已逐渐减少,被更安全的药物替代。
3. 广泛的工业与油田应用
油田钻井液添加剂:溴化钙溶液密度大(可达 1.8~2.3g/cm³),作为高密度钻井液(完井液)的主要成分,能平衡地层压力,防止井喷,同时对油气层损害小,适用于深井、高压油气井作业。
工业阻燃剂:与其他溴化物协同作用时,可增强材料的阻燃性能,用于塑料、纺织品等的防火处理。
制冷剂与除冰剂:其水溶液冰点低,可作为制冷剂的辅助成分;在道路除冰中,能降低冰雪熔点,提高除冰效率(但应用较少,因成本高于氯化钙)。
4. 易与其他物质发生反应
与硝酸银(AgNO₃)反应生成淡黄色溴化银(AgBr)沉淀,这是检验溴离子的反应:
CaBr₂ + 2AgNO₃ = 2AgBr↓ + Ca(NO₃)₂
与浓硫酸共热时,会发生氧化还原反应,生成溴单质(Br₂)、硫酸钙和水,体现溴离子的还原性。
5. 安全性需注意
溴化钙本身毒性较低,但过量摄入会导致溴中毒,出现头痛、嗜睡、精神错乱等症状,需严格控制使用剂量。
其粉尘或溶液对眼睛、皮肤有刺激性,接触后需及时用清水冲洗;储存时需与强酸、氧化剂分开,避免发生危险反应。